-
财经聚焦 普通会员【复星医药:Tenapanor片用于终末期肾病透析患者高磷血症治疗获临床试验注册审评受理】
12月5日丨复星医药公布,近日,公司控股子公司上海复星医药产业发展有限公司(“复星医药产业”)收到《受理通知书》(受理号:JXHL1900345国、JXHL1900346国、JXHL1900347国),其获许可的Tenapanor片(规格:10mg/20mg/30mg)用于终末期肾病透析患者高磷血症(ESRD-HD)治疗获国家药品监督管理局(“国家药监局”)临床试验注册审评受理。
2017年12月,复星医药产业获Ardelyx, Inc.(“Ardelyx”)关于该新药在区域内(包括中国大陆、香港及澳门特别行政区,下同)的独家临床开发和商业化等许可,Ardelyx仍为该新药在区域内的权利人。该新药为化学药品,主要用于治疗便秘性肠易激综合症和终末期肾病透析患者高磷血症。
2019年9月,该新药用于便秘性肠易激综合症治疗获国家药监局临床试验注册审评受理;同月,Ardelyx的Tenapanor片用于便秘性肠易激综合症治疗获美国食品和药品监督管理局(“美国FDA”)上市批准。
截至公告日,Ardelyx的Tenapanor片用于终末期肾病透析患者高磷血症治疗尚处于美国III期临床试验阶段。
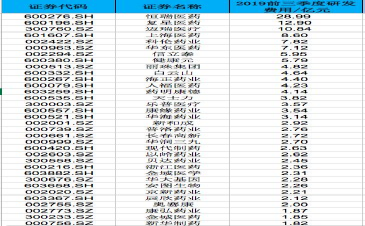
截至公告日,于中国境内(不包括港澳台地区,下同)上市的用于终末期肾病透析患者高磷血症治疗的药品包括Renvela®(Sevelamer,司维拉姆)和Fosrenol®(Lanthanum,碳酸镧)。根据IQVIA CHPA最新数据(由IQVIA提供,IQVIA是全球领先的医药健康产业专业信息和战略咨询服务提供商),2018年度,上述药品于中国境内的销售额为人民币约35,322万元。
截至2019年10月,集团现阶段针对该新药(用于便秘性肠易激综合症和终末期肾病透析患者高磷血症治疗)累计研发投入为人民币约9947万元(未经审计;包括许可费)。
-
-
-
-
-
-
-
-
财经聚焦 普通会员【复星医药:桂林南药阿莫西林胶囊通过仿制药一致性评价】
12月3日丨复星医药公布,近日,公司控股子公司桂林南药股份有限公司(以下简称“桂林南药”)收到国家药品监督管理局颁发的关于阿莫西林胶囊的《药品补充申请批件》(批件号:2019B04284),该药品通过仿制药一致性评价。
阿莫西林胶囊片主要用于敏感菌(不产β内酰胺酶菌株)所致的成人与儿童的感染。2018年度,桂林南药阿莫西林胶囊于中国境内(不包括港澳台地区,下同)的销售额约为人民币1245万元(未经审计)。
截至本公告日,于中国境内已上市的阿莫西林制剂主要包括香港联邦制药有限公司的阿莫仙®、山西同达药业有限公司的阿莫西林等。根据IQVIACHPA最新数据(由IQVIA提供,IQVIA是全球领先的医药健康产业专业信息和战略咨询服务提供商),2018年度,阿莫西林制剂于中国境内销售额约为人民币2.28亿元。截至2019年11月,桂林南药现阶段针对该药品一致性评价累计研发投入人民币约655万元(未经审计)。
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
xb337826003 普通会员
关于复星医药估值复星医药因为业务延绵整个医药行业,估值较为复杂。我试着以涉及的医药子行业和投资已上市企业分别估值。1、制药(主要是药友、万邦、奥鸿等)这部分19年毛估营收230亿,净利润20亿左右,参 详情
 新消息提醒
新消息提醒
聊吧群聊
-
1
问:复星医药展望2020,复星医药未来发展?
答:公司未来发展的讨论与分析 ...详情>>
- 2
-
3
问:复星医药2024年业绩预告?
答:复星医药公司 2023-12-31 财务...详情>>
- 4
- 5


 技术分析——选 《赢家江恩软件》>>
技术分析——选 《赢家江恩软件》>>