-
伯乐相马 普通会员复星医药午后大幅拉升,截至发稿,涨幅已超6%,总市值943亿。
-
-
Resolut1on 普通会员
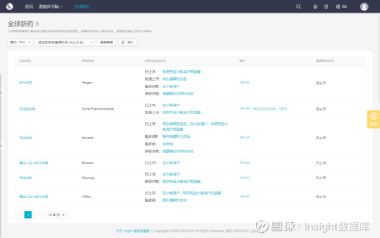
标题复星利妥昔单抗注射液增产获批加速抢占研药市场来源新京报新京报讯(记者王卡拉)4月15日,复星医药发布公告,其自主研发的单克隆抗体药物利妥昔单抗注射液(商品名汉利康)获批增加液2000L 详情
-
财经聚焦 普通会员【复星医药:汉霖制药获药品补充申请批件】
4月14日丨复星医药公布,近日,公司控股子公司上海复宏汉霖生物制药有限公司(以下简称“汉霖制药”)收到国家药品监督管理局颁发的关于利妥昔单抗注射液(即重组人鼠嵌合抗CD20单克隆抗体注射液,商品名称:汉利康®)的《药品补充申请批件》,获批增加原液2000L生产规模及2000L生产设备等。
该新药为集团(即公司及控股子公司/单位,下同)自主研发的单克隆抗体药物,主要适用于非霍奇金淋巴瘤、类风湿关节炎的治疗。2019年度,集团汉利康?于中国境内(不包括港澳台地区,下同)的销售额约为人民币1.5亿元。
截至本公告日,于中国境内上市的利妥昔单抗注射液为上海罗氏制药有限公司的美罗华®、汉霖制药的汉利康®(均用于非霍奇金淋巴瘤适应症)。根据IQVIACHPA最新数据(由IQVIA提供,IQVIA是全球领先的医药健康产业专业信息和战略咨询服务提供商),2019年度,利妥昔单抗注射液于中国境内销售额约为人民币25.05亿元。
截至2020年3月,集团现阶段针对该新药(包括非霍奇金淋巴瘤适应症及类风湿关节炎适应症)已投入研发费用人民币约5.95亿元(未经审计)。
-
-
-
-
-
-
-
-
神在人间TDS 普通会员早盘三大指数弱势震荡,医药股走强领涨盘面,人民同泰、未名医药涨停,智飞生物、华兰生物、复星医药等集体跟涨。
-
-
-
-
-
-
财经聚焦 普通会员【复星医药:重组抗CTLA-4全人单克隆抗体注射液获药品临床试验通知书】
4月8日丨复星医药公布,近日,公司控股子公司上海复宏汉霖生物技术股份有限公司(“复宏汉霖”)及上海复宏汉霖生物制药有限公司(“汉霖制药”)收到国家药品监督管理局关于同意其研制的重组抗CTLA-4全人单克隆抗体注射液(生物类似药,即HLX13;“该新药”)用于无法切除或转移性黑色素瘤、晚期肾细胞癌、微卫星高度不稳定性或错配修复缺陷的转移性结直肠癌治疗以及黑色素瘤辅助治疗开展临床试验的通知书。复宏汉霖及汉霖制药拟于近期条件具备后于中国境内(不包括港澳台地区,下同)开展该新药的临床I期试验。
该新药为集团自主研发的伊匹木单抗生物类似药,主要用于无法切除或转移性黑色素瘤、晚期肾细胞癌、微卫星高度不稳定性或错配修复缺陷的转移性结直肠癌治疗以及黑色素瘤辅助治疗。
截至公告日,于全球上市的CTLA-4靶点的单克隆抗体药品为Bristol-Myers Squibb的Yervoy®(Ipilimumab),于中国境内尚无同靶点的同类药物上市。根据IQVIAMIDASTM最新数据(由IQVIA提供,IQVIA是全球领先的医药健康产业专业信息和战略咨询服务提供商),2019年度,Yervoy®(Ipilimumab)于全球销售额约15.23亿美元。
截至2020年3月,集团现阶段针对该新药累计研发投入为人民币约2422万元(未经审计)。
-
-
-
-
-
-
-
 新消息提醒
新消息提醒
聊吧群聊
- 1
-
2
问:复星医药2024年业绩预告?
答:复星医药公司 2023-12-31 财务...详情>>
- 3
-
4
问:复星医药属于什么板块?
答:复星医药所属板块是 上游行业...详情>>
- 5


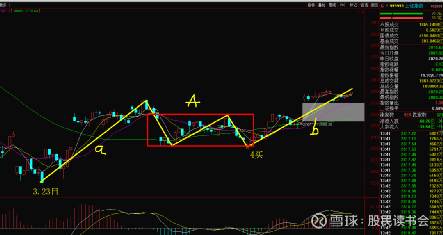
 技术分析——选 《赢家江恩软件》>>
技术分析——选 《赢家江恩软件》>>