-
财经聚焦 普通会员【亿帆医药:9月8日首次回购150万股】
9月8日丨亿帆医药公布,2021年9月8日,公司首次通过回购专用证券账户以集中竞价交易方式回购公司股份150万股,占公司目前总股本的0.12%,最高成交价为17.83元/股,最低成交价为17.35元/股,成交均价为17.60元/股,支付的总金额为2640.48万元(不含交易费用)。
-
财经聚焦 普通会员【亿帆医药:在研产品F-652新增适应症慢加急性肝衰竭获批开展II期临床试验】
9月7日丨亿帆医药公布,公司控股子公司亿一生物医药开发(上海)有限公司(“上海亿一”)于2021年9月7日收到国家药品监督管理局核准签发的《药物临床试验批准通知书》,同意上海亿一就在研产品重组人白介素22-Fc融合蛋白(“F-652”)新增适应症慢加急性肝衰竭开展II期临床试验。
审批结论: 根据《中华人民共和国药品管理法》及有关规定,经审查,2021年6月22日受理的注射用重组人白介素22-Fc融合蛋白符合药品注册的有关要求,同意开展临床试验。
-
-
财经聚焦 普通会员【亿帆医药:截至8月底尚未开始回购股份】
9月2日丨亿帆医药公布,公司于2021年8月26日召开第七届董事会第十九次会议,审议通过了《关于回购公司股份方案的议案》,公司拟使用自有资金以集中竞价交易的方式回购公司股份用于股权激励或员工持股计划,回购股份的资金总额为不低于1亿元(含)且不超过1.5亿元(含),回购价格不超过21.88元/股。截至2021年8月31日,公司尚未开始回购股份。
-
-
-
-
-
-
-
-
财经聚焦 普通会员【亿帆医药:624.075万股限制性股票将于7月15日上市流通】
7月12日丨亿帆医药发布关于2019年限制性股票激励计划首次授予部分第二个解除限售期解除限售股份上市流通的提示性公告,本次符合解除限售条件的激励对象共计184名,本次解除限售限制性股票数量为624.075万股,占公司目前总股本的0.5057%。
据悉,本次限制性股票来源为公司向激励对象定向发行公司的股票,解除限售的限制性股票将于2021年7月15日上市流通。
-
财经聚焦 普通会员【亿帆医药半年度净利润预降65%-75%】
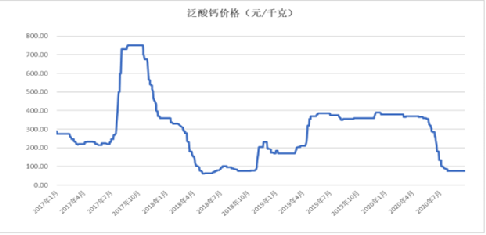
7月12日丨亿帆医药公布,预计2021年半年度归属于上市公司股东的净利润17959.18万元至25142.85万元,同比下降65%-75%。主要原因为报告期内公司原料药业务主要产品价格同比上年下降较大及海外业务较上年同期利润下降较大所致。
-
-
财经聚焦 普通会员【亿帆医药:可解除限售的限制性股票为624.08万股】
6月24日丨亿帆医药公布,公司2019年限制性股票激励计划首次授予部分第二个解除限售期解除限售条件已经成就,符合解除限售条件的激励对象共计184名,可解除限售的限制性股票数量为624.08万股,占公司目前总股本的0.51%;
此次限制性股票办理完解除限售手续后,在上市流通前,公司将发布相关提示性公告,敬请投资者注意。
-
财经聚焦 普通会员【亿帆医药:控股股东程先锋解质1400万股】
6月8日丨亿帆医药公布,公司于2021年6月8日收到公司控股股东程先锋的通知,获悉程先锋将其持有的公司股份部分办理了解除质押业务,此次解除质押股份1400万股。
-
财经聚焦 普通会员【亿帆医药:控股股东程先锋质押1500万股】
6月7日丨亿帆医药公布,公司于近日收到公司控股股东程先锋的通知,获悉程先锋将其持有的公司股份部分办理了质押业务,此次质押股份1500万股。
截至公告披露日,程先锋及其一致行动人合计持有公司股份521,196,307股,占公司总股本的42.21%,累计质押公司股份73,270,000股,占其持有公司股份总数的14.06%,占公司总股本的5.93%。
-
-
财经聚焦 普通会员【亿帆医药:FDA正式接受F-627的上市申请】
5月28日丨亿帆医药公布,公司控股子公司Evive Biotech Ltd. (“亿一生物”,含其下属子公司,下同)自主研发的在研品种重组人粒细胞集落刺激因子-Fc融合蛋白(“F-627”)用于预防及治疗肿瘤患者在化疗过程中引起的嗜中性粒细胞减少症于北京时间2021年5月27日晚收到美国食品药品管理局(FDA)的受理函,正式接受F-627的上市申请,标志着F-627正式进入技术审核阶段。
受理函结论:FDA已经完成了文件审查,并确定亿一生物的申请材料符合进行实质性审查的要求。按照21 CFR 601.2 (a)的规定,FDA正式接受亿一生物BLA申请。根据申请的内容,亿一生物的申请符合Prescription Drug User Fee Act (PDUFA) VI 法规中“标准”审批的规定,审批目标日期为2022年3月30日。
此次FDA接受F-627的上市申请,正式进入技术审核阶段,是其实现国际化创新征途上的又一重要里程碑事件,证明了亿一生物已经跻身于国际化生物制药企业的行列并具备了全球研发、临床、申报和生产的综合经验以及能力;更预示着中国生物创新药企有能力满足FDA的严格监管要求,把创新成果带到全球市场。
F-627是基于亿一生物现有具有自主知识产权Di-KineTM双分子技术平台开发的创新生物药品种。是基于Fc融合蛋白技术,由CHO细胞表达的rhG-CSF二聚体,具有长效和强效的生物学特点。目前F-627主要应用于预防及治疗肿瘤患者在化疗过程中引起的嗜中性粒细胞减少症,可使肿瘤化疗患者嗜中性粒细胞迅速增殖和恢复,从而增强了免疫系统抵抗感染的能力,以防止患者在化疗期间死于感染或者其他相关并发症。
2017年10月,F-627第二个国际III期临床试验(“05试验”)方案与FDA达成具有约束力的协议(SPA),表明FDA认可F-627的05临床试验方案和临床结果统计分析方法;2018年1月,亿一生物完成了F-627首个在美国开展的III期临床试验(“04试验”),并达到预设主要疗效终点,受试者耐受情况良好,安全性达到预期;2020年1月5日,亿一生物收到在中国开展的F-627的III期临床试验《统计数据图表合集》,统计结果表明,F-627中国III期临床试验的有效性结果已全面达到临床试验预设评价标准,疗效与对照药品(原研进口药品重组人粒细胞集落刺激因子)相当;2020年6月,亿一生物收到在美国及欧洲开展的05试验《统计数据图表合集》,结果显示,第二个国际III期临床试验成功达到预设主要疗效终点和次要疗效终点,药物疗效与对照药品相当;2020年7月,公司完成了05试验有关免疫原性的中和抗体检测,结果为阴性,标志着无药物相关的抗体产生;自此,F-627国内外开展的I期、II期及III期临床试验,均圆满达到临床试验预设目标。2021年3月30日,F-627向美国FDA提交BLA申请。上述事项具体内容详见公司于2020年1月6日、2020年6月29日、2020年7月8日及2021年3月31日披露的《关于控股子公司在研产品F-627国内III期临床试验结果达到预设评价标准的公告》(公告编号:2020-001)、《关于控股子公司在研产品F-627国际III期关键性临床试验结果达到预设评价标准的公告》(公告编号:2020-044)、《关于控股子公司在研产品F-627第二个国际III期关键性临床试验结果的进展公告》(2020-046)及《关于控股子公司在研产品F-627项目的进展公告》(公告编号:2021-038)。
-
-
-
-
-
-
 新消息提醒
新消息提醒
聊吧群聊
-
1
问:亿帆医药有哪些子公司?
答:亿帆医药的子公司有:19个,分别...详情>>
-
2
问:亿帆医药股票持仓基金?
答:上海迎水投资管理有限公司-迎...详情>>
- 3
- 4
- 5


 技术分析——选 《赢家江恩软件》>>
技术分析——选 《赢家江恩软件》>>