- 全部
- 复盘
- 江恩分析
- 上市
- 产品
- 公告
- 分析
- 股价
- 主力
- 业绩
- 前景
- 看涨
- 董事长
- 股东
- 怎么样
- 涨停
- 年报
- 快讯
- 季报
- 基本面
- 利好
- 重组
- 股权
- 三季报
- 跌停
- 估值
- 产能
- 阻力位
- 看跌
- 利空
- 研报
- 收购
-
-
-
-
-
-
财经聚焦 普通会员【君实生物:JS014注射液开展晚期恶性肿瘤临床试验的申请获得批准】
8月31日丨君实生物公布,近日,公司收到国家药品监督管理局核准签发的《药物临床试验批准通知书》,JS014注射液(项目代号“JS014”)的临床试验申请获得批准。由于药品的研发周期长、审批环节多,容易受到一些不确定性因素的影响,敬请广大投资者谨慎决策,注意防范投资风险。
审批结论:根据《中华人民共和国药品管理法》及有关规定,经审查,2021年6月24日受理的JS014注射液符合药品注册的有关要求,同意本品开展晚期恶性肿瘤临床试验。
JS014注射液的活性成分为重组白介素 21-抗人血清白蛋白(HSA)纳米抗体融合蛋白,通过融合抗 HSA 的纳米抗体使 IL-21 的半衰期得到显著延长。该产品能以高亲和力特异性地结合人 IL-21R 并激活淋巴细胞,半衰期的延长可以提高药物在肿瘤微环境中的分布,增强肿瘤微环境中浸润淋巴细胞的活性,进而增强免疫系统杀伤肿瘤细胞的能力。此外,JS014与免疫检查点单抗联用体现出强大的协同抗肿瘤活性。
2019年6月,公司与Anwita Biosciences, Inc.签署《许可协议》,公司获得在大中华区(包括中国大陆、香港特别行政区、澳门特别行政区及台湾地区)开发及商业化创新IL-21融合蛋白JS014的权利。
-
-
-
-
-
-
-
-
-
-
-
财经聚焦 普通会员【君实生物半年报:营收同比增长267.77%、处于商业化阶段的在研产品共2项】
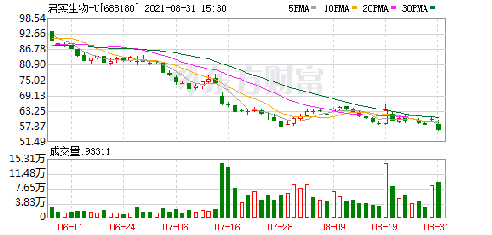
8月30日丨君实生物发布2021年半年度报告,实现营业收入21.14亿元,同比增长267.77%;归属于上市公司股东的净利润0.09亿元,归属于上市公司股东的扣除非经常性损益的净利润-1.13亿元,扣除非经常性损益后净利润仍为负数主要由于公司对在研项目研发投入的持续加大以及对商业化产品特瑞普利单抗的推广力度的加大。
报告期内,公司研发费用为9.47亿元,同比增长33.62%。研发费用增长主要由于公司在报告期内不断丰富和拓展在研产品管线,快速推进现有临床项目的开展,持续探索药物在临床阶段的联合治疗方案所致。报告期内,公司销售费用为4.23亿元,与上年同期相比增长85.22%。随着特瑞普利单抗的准入医院数量及覆盖药房数量大幅度增加,公司商业化团队一线销售人员扩充以及商业化推广力度加大导致销售费用相应增长。
公司是一家创新驱动型生物制药公司,具备完整的从创新药物的发现和开发、在全球范围内的临床研究、大规模生产到商业化的全产业链能力。
公司旨在通过源头创新来开发first-in-class(同类首创)或best-in-class(同类最优)的药物,通过卓越的创新药物发现能力、强大的生物技术研发能力、大规模生产技术,已成功开发出极具市场潜力的在研药品组合,多项产品具有里程碑意义:核心产品之一特瑞普利单抗是国内首个获得国家药监局批准上市的国产抗PD-1 单克隆抗体;昂戈瑞西单抗和UBP1213 是中国本土公司首次获得国家药监局IND 批准的抗PCSK9 单克隆抗体和抗BLyS 单克隆抗体;TAB004/JS004 是公司自主研发、全球首创的抗BTLA 单克隆抗体,已获得FDA 和NMPA 的临床试验批准,目前正在中美两地开展临床试验;公司还与国内科研机构携手抗疫,共同开发新冠病毒中和抗体JS016,用本土创新为中国和世界疾病预防控制贡献力量,目前已获得美国FDA 紧急使用授权。公司的创新研发领域已经从单抗药物类型扩展至包括小分子药物、多肽类药物、抗体药物偶联物(ADCs)、双特异性或多特异性抗体药物、核酸类药物等更多类型的药物研发以及癌症、自身免疫性疾病的下一代创新疗法探索。
公司的核心团队成员均来自于行业知名机构、跨国企业或监管机构,具有良好的教育背景和丰富的研发、注册、质量管理、生产、销售与公司治理经验。依托优秀的人才储备和持续的资金投入,公司已建立全球一体化的研发流程,并于美国的旧金山、马里兰以及国内的上海及苏州都设有研发中心。公司自主开发并建立了涵盖蛋白药物从早期研发到产业化的整个生命周期的完整技术体系,该体系包括多个技术平台:(1)抗体筛选及功能测定的自动化高效筛选平台、(2)人体膜受体蛋白组库和高通量筛选平台、(3)抗体人源化及构建平台、(4)高产稳定表达细胞株筛选构建平台、(5)CHO 细胞发酵工艺开发平台、(6)抗体纯化工艺及制剂工艺开发与配方优化平台、(7)抗体质量研究、控制及保证平台、(8)抗体偶联药研发平台、(9)siRNA 药物研发平台。
公司拥有2个生产基地。苏州吴江生产基地已获GMP认证,拥有4500L发酵能力,其中3000L发酵能力可用于公司产品的商业化生产和临床试验用药的生产,报告期内新增1500L发酵能力,用于支持阿达木单抗的原液生产及其他在研药物的临床试验用药生产。上海临港生产基地按照CGMP标准建设,其中一期项目产能30000L,已于2019 年底投入试生产,目前正在进行特瑞普利单抗的技术转移工作,并在报告期内支持了JS016项目的临床试验样品在全球临床试验的供药和原液供应。由于规模效应,临港生产基地产能的扩充亦将为公司带来更具竞争力的生产成本,并通过更多临床试验加速推出新药物。根据目前在研产品管线的研发进度,公司计划进一步扩展我们的生产设施,以提供可与公司日益增长及渐趋成熟的在研药物相匹配的充足产能,并支持公司的业务在未来的持续扩张。 公司高度重视知识产权保护,设置专利部门负责境内外专利的申报与维护工作。
截至报告期末,公司拥有86项已授权专利,其中66项为境内专利,20项为境外专利。专利覆盖新药蛋白结构、制备工艺、用途、制剂配方等,为公司产品提供充分的和长生命周期的专利保护。
截至公告披露日,公司在研产品管线覆盖五大治疗领域,包括恶性肿瘤、自身免疫系统疾病、慢性代谢类疾病、神经系统类疾病以及感染类疾病。其中,处于商业化阶段的在研产品共2项(特瑞普利单抗以及埃特司韦单抗),处于新药上市申请阶段在研产品1项(阿达木单抗),除上述产品外另有16项在研产品处于临床试验阶段(其中PARP 抑制剂、昂戈瑞西单抗以及贝伐珠单抗处于三期临床试验阶段),25项在研产品处在临床前开发阶段。
-
-
-
-
-
yuuvvgghcfcc 普通会员
“千山暮雪1”提问注意到大宗交易中招商证券有限公司龙口港城大道证券营业部近一个多月以来通过大宗交易减持公司股份数量超过了2%,请问其是不是公司持股比例超过5%的大股东或者公司公司高管? 详情
-
-
-
 新消息提醒
新消息提醒
聊吧群聊
- 1
- 2
-
3
问:君实生物2024年业绩预告?
答:君实生物公司 2023-12-31 财务...详情>>
- 4
-
5
问:君实生物属于什么板块?
答:君实生物所属板块是 上游行业...详情>>


 技术分析——选 《赢家江恩软件》>>
技术分析——选 《赢家江恩软件》>>