-
-
-
财经聚焦 普通会员【博晖创新:人凝血因子Ⅷ获批药物临床试验】
5月25日丨博晖创新公布,公司控股子公司河北大安制药有限公司(“大安制药”)研发的人凝血因子VIII于近日获得了国家药品监督管理局颁发的《药物临床试验批准通知书》。
临床试验开展前,请申请人与研究者讨论,进一步修订完善本品临床试验方案,建议如下:1、PK 试验:先完成至少12 例受试者单次给药PK 试验再进行按需治疗研究,以便根据PK 试验结果设置有效性研究的活性回收率采样时间点;完成PK 试验的受试者可继续进行按需治疗研究;请明确PK 试验期间若受试者发生出血的治疗方案。2、主要疗效指标:根据止血疗效四级评分量表,止血疗效评价时间点至少应包括每次出血治疗第1 次给药后的8hr和72hr。3、因子VIII抑制物:(1)为避免因输注因子VIII而影响低水平抑制物的发现,建议在抑制物检测用血样采集前至少48h 不输注因子VIII,以保证至少5 个半衰期的洗脱期;(2)中心实验室应对抑制物进行及时检测,不可将首次用药后第90天的抑制物检测放在180 天检测,以便及早发现抑制物发生情况;(3)若检测到抑制物,建议在1-4 周内再次检测抑制物;(4)明确受试者出现抑制物时的治疗措施。4、本临床试验纳入的受试者为先天性血友病A 患者,建议删除方案中获得性因子VIII抑制物增多症的适应症及相关给药方案。
临床试验期间,申请人可就试验中相关问题向药品审评中心提出沟通交流会议申请。
本项临床试验应当在批准之日起3 年内实施,逾期未实施的,本件自行废止。
-
不求涨停%但求涨个不停! 普通会员
“irm1189928”提问公司与其他血制品上市公司相比,优势和略少分别是什么?请介绍。公司官方回答尊敬的投资者,你好。公司自进入血液制品板块以来,持续加大投入,拓展浆源,丰富产品 详情
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
 新消息提醒
新消息提醒
聊吧群聊
- 1
- 2
-
3
问:博晖创新2024年业绩预告?
答:博晖创新公司 2024-03-31 财务...详情>>
-
4
问:博晖创新有哪些子公司?
答:博晖创新的子公司有:6个,分别...详情>>
- 5


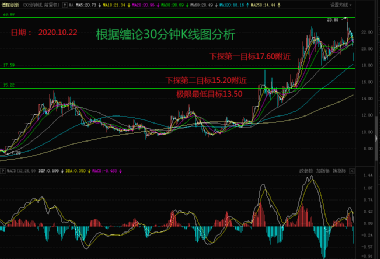
 技术分析——选 《赢家江恩软件》>>
技术分析——选 《赢家江恩软件》>>