-
-
用户1630173452 普通会员
“irm7532728”提问请问带量采购对公司盈利有何影响?公司官方回答您好,目前国家层面的注射剂集采尚未开展,未来将与一致性评价审评审批步伐相对统一。公司已根据带量采购的节奏、范 详情
-
-
lonelypisces 普通会员【奥赛康:子公司创新药ASKB589获得临床试验批准通知书】奥赛康公告,公司及其全资子公司奥赛康生物于近日收到国家药品监督管理局下发的ASKB589注射液《药物临床试验批准通知书》。ASKB589 注射液为江苏奥赛康自主研发、具有自主知识产权的抗肿瘤生物新药,其主要通过ADCC和CDC杀伤肿瘤细胞,拟用于胃及胃食管结合部腺癌、胰腺癌等适应症。
-
我的人生彩虹 普通会员【奥赛康:子公司创新药ASKB589获得临床试验批准通知书】奥赛康公告,公司及其全资子公司奥赛康生物于近日收到国家药品监督管理局下发的ASKB589注射液《药物临床试验批准通知书》。ASKB589 注射液为江苏奥赛康自主研发、具有自主知识产权的抗肿瘤生物新药,其主要通过ADCC和CDC杀伤肿瘤细胞,拟用于胃及胃食管结合部腺癌、胰腺癌等适应症。
-
微尘r 普通会员【奥赛康:注射用格列本脲通过临床试验申请】奥赛康公告,公司全资子公司江苏奥赛康药业有限公司于近日收到国家药品监督管理局下发的注射用格列本脲新药临床试验申请《受理通知书》。注射用格列本脲是一种选择性磺脲类受体1(SUR1)抑制剂,通过阻断SUR1-TRPM4(瞬时受体电位M4)通道发挥神经保护作用。
-
zhoubo0710 普通会员
首先复盘我们的票。1、禾丰牧业(2020.4.9日关注)。长期持有暂不管他震荡,若回调到20日线,老A就补仓。2、奥赛康(2020.4.14日关注)。短期走势与禾609差不多,都是属于前期上涨后短期回 详情
-
-
财经聚焦 普通会员【奥赛康2019年度净利润升16.55%至7.81亿元 拟10派2.2元】
4月29日丨奥赛康发布2019年年度报告,实现营业收入45.19亿元,同比增长14.92%;归属于上市公司股东的净利润7.81亿元,同比增长16.55%;归属于上市公司股东的扣除非经常性损益的净利润7.61亿元,同比增长18.78%;基本每股收益0.84元,拟每10股派发现金红利2.2元(含税)。
公司专注于抗消化道溃疡、抗肿瘤、抗耐药菌感染、慢性病等领域的产品研发、生产、销售,在中国医药细分市场具有较高的品牌影响力,产品定位于临床亟需、国内首仿、创仿结合,产品剂型主要定位于冻干粉针制剂、小容量注射剂、固体口服制剂,目前在中国抗消化性溃疡质子泵抑制剂注射剂产品的细分领域市场占有率第一,是该细分领域的龙头企业。奥赛康药业在长期的发展过程中,逐步创建了“以健康为本的‘头尾创新’的奥赛康管理模式”,既重视“头部创新”,重点抓研发和技术突破,又重视“尾部创新”,强调工艺改进、质量提升,使“尾部创新”与“头部创新”互相融合、相得益彰,实现公司高质量、可持续健康发展。
报告期内,公司新品沙格列汀片、注射用帕瑞昔布钠的顺利上市,标志着奥赛康药业扩展了新的剂型,进军新的治疗领域,公司发展迈上新台阶。
-
财经聚焦 普通会员【奥赛康一季度净利润降43.35%至1.07亿元】
4月29日丨奥赛康发布2020年第一季度报告,实现营业收入7.09亿元,同比下降36.31%;归属于上市公司股东的净利润1.07亿元,同比下降43.35%;归属于上市公司股东的扣除非经常性损益的净利润1.02亿元,同比下降43.11%;基本每股收益0.11元。
-
-
财经聚焦 普通会员【奥赛康:ASKB589注射液的新药临床试验申请获受理】
4月13日丨奥赛康公布,公司的全资子公司江苏奥赛康药业有限公司(“江苏奥赛康”)及其全资子公司江苏奥赛康生物医药有限公司(“奥赛康生物”)于近日收到国家药品监督管理局下发的ASKB589注射液新药临床试验申请《受理通知书》。
ASKB589注射液为江苏奥赛康自主研发、具有自主知识产权的抗肿瘤生物新药,其主要通过ADCC和补体依赖的细胞毒作用(CDC)杀伤肿瘤细胞,拟用于胃及胃食管结合部腺癌、胰腺癌等适应症。
中国胃癌的发病率和死亡率在所有恶性肿瘤中排名第二,临床上发现的胃癌多为局部晚期或晚期,且目前胃癌化疗和靶向治疗药物种类及作用均有限。胰腺癌具有恶性程度较高、进展迅速、起病隐匿以及早期症状不典型等特点,临床就诊时大部分患者已属于中晚期。胰腺癌的5年相对生存率在常见恶性肿瘤中最差,仅为7.2%,且呈逐年恶化的趋势。目前手术切除依然是胰腺癌患者获得治愈机会和长期生存的唯一有效方法,以吉西他滨为基础的药物化疗是晚期胰腺癌最主要的一线治疗方式。
江苏奥赛康、奥赛康生物目前完成了ASKB589注射液的药学研究、药理毒理研究以及临床试验方案设计,向药监局提交了临床试验申请(IND)并获得正式受理。现有研究结果表明,ASKB589注射液与靶点结合具有高度特异性,与化疗药物联用治疗胃及胃食管结合部腺癌、胰腺癌等恶性实体瘤具有良好的开发前景。
该产品已投入研发费用约7464.39万元人民币,国内外尚无同类产品获批上市。根据我国药品注册相关的法律法规要求,药物经国家药监局审评审批通过后方可开展临床试验。如顺利通过审批将进一步丰富公司产品线,增强公司市场竞争力。
-
-
财经聚焦 普通会员【奥赛康:获得地拉罗司分散片和地拉罗司原料药生产注册受理通知书】
3月5日丨奥赛康公布,公司的全资子公司江苏奥赛康药业有限公司(“江苏奥赛康”)于近日收到国家药品监督管理局下发的地拉罗司分散片注册《受理通知书》;江苏奥赛康的子公司南京海润医药有限公司(“南京海润”)于近日收到国家药品监督管理局下发的地拉罗司原料药登记生产的《受理通知书》。
地中海贫血又称海洋性贫血,在地中海、东南亚等地区多见,是一组严重威胁人类健康的致死、致残的遗传性血液病。据《中国地中海贫血蓝皮书(2015)》介绍,我国重型和中间型地贫患者在30万人左右。输血是治疗重型和中间型地中海贫血的主要措施。另外,输血也是骨髓增生异常综合征(MDS)主要的维持疗法,我国每年约有30万例左右新发MDS患者。长期输血易导致继发性铁过载,铁过载是指过多的铁沉积在人体组织器官,导致细胞损伤和器官功能障碍的病理现象,铁过载可对心血管、内分泌、肝脏、肾脏、神经系统等产生损害,导致多种疾病,危害严重。铁螯合剂可有效地提高铁的排泄,降低体内铁的含量及其在各器官的病理性沉积,地拉罗司是目前治疗铁过载唯一有效的药物。
地拉罗司是FDA在2005年批准的第一个能够常规使用的口服铁螯合剂,FDA授予地拉罗司治疗非输血依赖地中海贫血铁过载的孤儿药地位,目前已在80多个国家上市。在美国上市的口服混悬液和分散片,被批准用于治疗2岁及以上的成年和小儿患者因输血而引起的慢性铁过载,和10岁以上非输血依赖性地中海贫血(NTDT)综合征患者的慢性铁过载。2012年,地拉罗司在欧盟被批准用于6岁及以上因频繁输血(红细胞压积≥7ml/kg/月)而导致慢性铁过载地中海贫血患者的治疗,还被批准用于治疗去铁胺治疗被禁忌或不足时,因输血引起的慢性铁过载。在日本,本品被批准用于治疗因输血引起的铁过载。
2010年,地拉罗司分散片在中国获批上市,被批准用于年龄大于2岁及的β地中海贫血患者因频繁输血而引起的慢性铁过载,和10岁及10岁以上非输血依赖性地中海贫血(NTDT)综合征患者的慢性铁过载的治疗。它的优点是能清除游离铁、细胞内铁,并能阻止心肌细胞摄取铁,直接从心肌细胞去除多余的铁,使得血浆中非转铁蛋白持续减少,是输血导致的慢性铁过载患者的一线用药。地拉罗司分散片可以一日一次口服用药,患者顺应性好,保证祛铁治疗得以长期进行。上述地拉罗司的良好祛铁有效性、安全性和患者顺应性,大大降低了地中海贫血、MDS等需要长期输血治疗的疾病患者的死亡率,并提高了他们的生活质量。
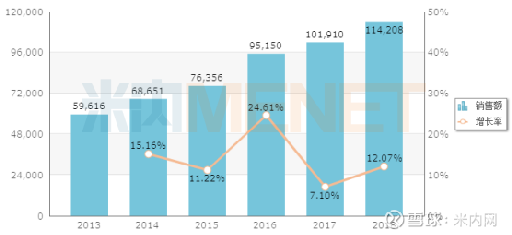
2019年地拉罗司分散片通过国家谈判进入了最新版医保目录;诺华制药的地拉罗司2019年的全球销售额达9.75亿美元;PDB数据库显示,2019年前三季度地拉罗司国内销售额为:700.29万元。
地拉罗司分散片被列入了国家卫健委发布的《第一批鼓励仿制药品目录》,江苏奥赛康研发的地拉罗司分散片于2018年获得国家“十三五”“重大新药创制”科技重大专项课题立项,系国内首家完成临床生物等效性研究并提交生产注册申请的公司。
截至目前,该产品已投入研发费用约1809万元人民币。根据我国药品注册相关的法律法规要求,药物经国家药监局审评审批通过后方可生产上市。如顺利通过审批将进一步丰富公司产品线,增强公司市场竞争力。
-
-
-
-
-
-
-
财经聚焦 普通会员【奥赛康:拟5000万元向扬州三药增资】
12月24日丨奥赛康公布,公司的子公司江苏奥赛康药业有限公司(“江苏奥赛康”或“子公司”)拟以自有资金5000万元向扬州市三药制药有限公司(“扬州三药”)增资。
增资完成后,江苏奥赛康将获得扬州三药20%股权。江苏奥赛康与扬州三药及其股东汤中信、汤俊、解家顺、李玉江于2019年12月24日签署了《投资协议书》。
公司及子公司专注于中国医药的主要细分市场,目前产品剂型主要定位于冻干粉针制剂、固体口服制剂。借助扬州三药丰富的固体口服产品生产管理经验,厂房及公共配套设施、完备的产业和技术工人,能够快速高质量地打造子公司的固体口服在研产品的中试研发基地和固体口服制剂的产业化基地,来满足子公司在研产品后续产业化的研发进度和产能需求。在保持冻干粉针剂优势的基础上,进一步开展公司及子公司在固体口服制剂领域的产品布局,满足临床用药需求,增强企业竞争力,形成新的经济增长点。
此次对外投资紧紧围绕公司及子公司的主营业务展开,有效运行后将对公司及子公司的长远发展和企业效益将产生积极影响。投资资金来源为子公司的自有资金,不会对公司及子公司财务及经营状况产生不利影响,不存在损害公司及全体股东利益的情形。
-
-
-
-
财经聚焦 普通会员【奥赛康:拟获授予泊沙康唑肠溶片在中国大陆地区独家推广、商业及代理销售权益】
12月13日丨奥赛康公布,2019年12月12日,公司的子公司江苏奥赛康药业有限公司(“江苏奥赛康”)与上海宣泰医药科技有限公司(“上海宣泰”)签署了《关于泊沙康唑肠溶片产品独家代理销售事宜的合作意向书》。上海宣泰拟将拥有的泊沙康唑肠溶片(产品规格:100mg/片)在中国大陆地区(即中华人民共和国除香港特别行政区、澳门特别行政区及台湾以外的区域,“代理区域”)的独家推广、商业及代理销售权益授权江苏奥赛康。
产品获批适应症:用于预防侵袭性曲霉和念珠菌感染,适用于因免疫系统严重受损的患者,免疫系统严重受损包括造血干细胞移植(HSC T)接受者患有的移植物抗宿主病(GVHD)或恶性血液病患者因化疗而导致长期的中性粒细胞减少。
泊沙康唑肠溶片被列入国家发布的《第一批鼓励仿制药品目录建议清单》,作为新一代三唑类抗真菌药,泊沙康唑肠溶片用于预防侵袭性曲霉和念珠菌感染,适用于因免疫系统严重受损的患者,免疫系统严重受损包括造血干细胞移植(HSCT)接受者患有的移植物抗宿主病(GVHD)或恶性血液病患者因化疗而导致长期的中性粒细胞减少。随着癌症化疗、移植、HIV/AIDS感染以及糖尿病等高风险患者数量的不断增多,侵袭性真菌感染(IFIs)的总发病率不断攀升,一旦被感染,死亡率高达60%以上,泊沙康唑用于侵袭性真菌感染的预防具有区别于其它药物的治疗优势。与口服混悬液相比,肠溶片能够进一步提高口服生物利用度,使抗真菌效果更好得以发挥,服用也更加便捷,市场前景广阔。
目前上海宣泰的泊沙康唑肠溶片已于2019年8月21号获得美国FDA的ANDA批准,在美国上市销售。并且于2019年2月19日在国内报产,2019年9月16日进入优先审评名单,是国内独家完成生物等效性实验,首家申报生产的泊沙康唑肠溶片,预计2020年能够顺利上市。
江苏奥赛康研发的泊沙康唑注射液预计将于2020年国内首家上市,注射用多粘菌素E甲磺酸钠、注射用达托霉素、注射用伏立康唑等产品已经提交CDE报产等待审批,泊沙康唑肠溶片的上市将配合公司的产品布局,进一步巩固公司在耐药菌感染领域的地位,产生新的经济增长点。
 新消息提醒
新消息提醒
聊吧群聊
-
1
问:奥赛康有哪些子公司?
答:奥赛康的子公司有:2个,分别是:...详情>>
-
2
问:奥赛康展望2020,奥赛康未来发展?
答: 国家提出实施“健康中国”的...详情>>
- 3
- 4
- 5


 技术分析——选 《赢家江恩软件》>>
技术分析——选 《赢家江恩软件》>>